Las rutas metabólicas MTOR y AMPk son de suma importancia para el control del metabolismo y sus dos clásicas fases, el anabolismo (creación de tejido) y el catabolismo (destrucción del mismo) pero también para el desarrollo de patologías. Conocerlas y estudiarlas puede darnos armas terapéuticas para el cáncer o la diabetes.
La ruta del AMPk actúa más bien como un sensor energético de nuestro organismo. Detecta cuando tenemos déficit de ATP (nuestra moneda energética) y pone en marcha los mecanismos para obtenerla de nuevo por medio de la oxidación de ácidos grasos en músculo e hígado, mejora de la resistencia a la insulina y la entrada de glucosa en el músculo e inhibición de la síntesis de triglicéridos.
Dr. Alfonso Galán González – Equipo Médico Neolife
Un exceso de activación de la ruta MTOR puede llevar a cáncer, resistencia a la insulina, diabetes, alzheimer y parkinson, entre otras.
Como prometimos en estas mismas páginas en entradas previas del blog, vamos a explicar un poco más sobre estas dos rutas metabólicas, las del AMPk y MTOR, de suma importancia en el control del metabolismo y las dos fases del mismo, anabolismo (creación de tejido) y catabolismo (destrucción del mismo); pero también con una influencia enorme en la patología, y no hablamos de patologías extrañas que nunca hemos oído mencionar, hablamos de cáncer, diabetes, enfermedad cardiovascular, alzheimer, parkinson, etc…
¿Interesado? Siga leyendo y le explicamos cómo se puede conseguir un equilibrio entre estas vías para vivir más y más sano (Xu J et al. 2012).
MTOR
Esta vía metabólica está formada por una serie de proteínas que regulan procesos tan importantes como la creación de tejido a través de la síntesis proteica y la hiperplasia celular, es por tanto una vía fundamentalmente anabólica. Su nombre se debe a que su descubrimiento vino de su relación con la Rapamicina y los efectos que la inhibición de esta vía con Rapamicina tiene sobre el aumento de la longevidad (Mammalian Target Of Rapamycin). Además de este fármaco, la regulan otros factores como la insulina, el IGF-1 (insulin-like Growth Factor-1), los aminoácidos (leucina), el ejercicio de fuerza, etc,…
Efectivamente, la inhibición de la ruta MTOR se ha ligado a un aumento de la longevidad de determinados organismos (Johnson SC et al. 2013). Al parecer, a nivel biológico, la creación de tejido está reñida con la longevidad, así animales que tienen crecimiento muy rápido tienen esperanzas de vida cortas (véase, por ejemplo un ratón vs un elefante). La síntesis proteica aumentada y la creación de tejido e hiperplasia celular son beneficiosos durante la vida juvenil para hacer crecer el organismo, pero posteriormente mantener activada esta vía tendría efectos negativos sobre la longevidad. ¿Esto quiere decir que la debemos inhibir siempre? No, el equilibrio es lo importante como empezamos diciendo. Hay determinadas situaciones donde activarla es muy necesario y las explicaremos a continuación.
La dieta rica en hidratos de carbono con la consiguiente elevación de los niveles de insulina, la disponibilidad de aminoácidos y la IGF-1 activan esta vía, mientras que la restricción calórica (de la que hemos hablado ampliamente en otros artículos), bajar el aporte de aminoácidos, sobre todo leucina y la mencionada Rapamicina la inactivarían.
Un exceso de activación de la ruta MTOR puede llevar a cáncer, resistencia a la insulina, diabetes, alzheimer, parkinson, etc.(Saxton RA et al. 2017).
En relación con el cáncer la ruta MTOR es compleja:
- La activación de esta vía por los mecanismos mencionados, hace que se activen oncogenes.
- Al inhibirse la autofagia, la capacidad de nuestro sistema para atacar las células tumorales también se altera.
- Se activan los procesos de angiogénesis, esto es, la creación de nuevos vasos que aporten sangre con nutrientes al tumor.
- Las modificaciones en el metabolismo energético de las células que hacen que pasen a quemar energía en ausencia de oxígeno (glucolisis anaeróbica) típica de las células tumorales.
En cuanto a su relación con el alzheimer y parkinson, la formación de aglomerados de proteínas típico de estas enfermedades (ovillos neurofibrilares y placas de B-amiloide) se favorece al activarse MTOR, pues lleva a la formación de proteínas e inhibe la autofagia (que es el mecanismo por el que la célula “reciclaría” estos aglomerados de proteínas).
Entonces ¿Qué puede tener de bueno MTOR con lo explicado?.
Activar esta vía en determinadas situaciones o momentos es muy beneficiosa también. Necesitamos tener creación de tejido y síntesis muscular para reparar, desarrollar músculo tras el ejercicio, para no perder masa muscular con los años (sarcopenia), para cicatrizar tras lesiones o intervenciones quirúrgicas, etc,….
AMPk
Esta ruta actúa más bien como un sensor energético de nuestro organismo. Detecta cuando tenemos déficit de ATP (nuestra moneda energética) y pone en marcha los mecanismos para obtenerla de nuevo por medio de la oxidación de ácidos grasos en músculo e hígado, mejora de la resistencia a la insulina y la entrada de glucosa en el músculo, inhibición de la síntesis de triglicéridos, colesterol y acúmulo de grasa en los adipocitos, etc. (Lin SC et al. 2018).
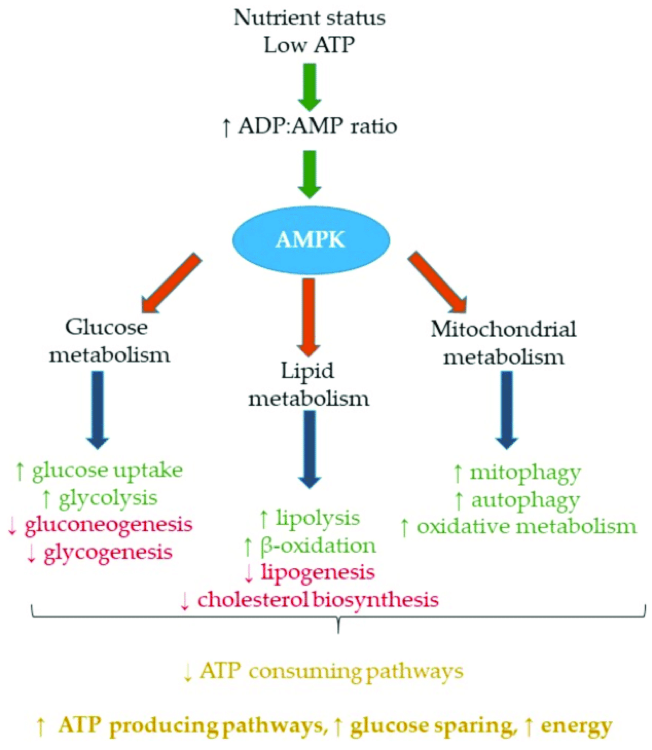
¿Qué activa la ruta AMPk?
-
Todo aquello que baje las concentraciones de ATP y aumente las de AMP (producto del uso de ATP para obtener energía) y aquellas situaciones que lleven a la célula a una situación de estrés (estrés oxidativo con aumento de especies reactivas del oxígeno y radicales libres, hipoxia, falta de glucosa,…) pueden producir un aumento de la ruta AMPk.
-
El Ejercicio, sobre todo el de alta intensidad (HIIT, Tabata..) hace que se active esta vía para obtener energía para su desempeño, esto explica parte de los efectos del ejercicio sobre la quema de grasas y su efecto para aumentar la sensibilidad a la insulina (Thompson DM et al. 2018).
-
Varias sustancias se han investigado para este fin. Mencionaremos, por ser las más reconocidas y usadas en la práctica, la metformina, la berberina, el resveratrol, la curcumina, el ácido alfa-lipoico y la cafeína.
- El ayuno, como forma de restricción calórica -principalmente implementado como ayuno intermitente-. A las 10-12 h de ayuno ya se activa esta vía.
Los efectos de la activación de esta vía son muchos, muy importantes y variados y ya los hemos dejado entrever.
- Al mejorar la resistencia a la insulina previene el desarrollo de diabetes tipo 2.
- Previene y mejora el hígado graso (la esteatosis hepática de origen no alcohólico) asociado al aumento de grasa visceral al promover la oxidación de los ácidos grasos e inhibir el depósito de grasa en los adipocitos.
- Promueve la biosíntesis mitocondrial y el metabolismo oxidativo a este nivel, esto es, hace que la central energética de nuestras células que son las mitocondrias, funcionen mejor e incluso hace que tengamos más de ellas para poder obtener más energía y de forma más eficiente, esto a nivel del músculo cardíaco hace que los procesos de muerte celular en respuesta a la isquemia cardíaca estén inhibidos y previene el daño cardíaco en estas situaciones.
- Se relaciona con otras hormonas importantes para la obtención de energía, como las catecolaminas (adrenalina y noradrenalina), el cortisol, las hormonas tiroideas T4 y T3 (fomentando también la conversión de T4 en T3, que es la hormona activa), el glucagón, la hormona del crecimiento y aumenta la producción de hormonas sexuales (Bertoldo MJ et al. 2015).
- Baja la inflamación al inhibir directamente NFKB, un activador de la inflamación. Pero los estados inflamatorios crónicos tienden a inhibirla (Jeon SM et al. 2016).
- En el síndrome de ovario poliquístico, que es un cuadro mucho más frecuente de lo que se piensa, donde la mujer puede sufrir una serie de alteraciones como la infertilidad, hirsutismo, obesidad, quistes ovárico, etc, pero sobretodo lo más constante de este síndrome es la resistencia a la insulina que, como hemos visto, puede mejorar activando la vía AMPk, de ahí que estas mujeres mejoren enormemente con metformina.
- La relación del AMPk con el cáncer se investiga desde hace más de 17 años cuando se descubrió su relación con oncogenes supresores como LKB1 y p53 (Ciccarese F et al. 2019), y la demostración de que activando esta vía se podía prevenir algunos tipos de cáncer o frenar su crecimiento. Pero, como todo, la relación es más compleja, implicando la autofagia y el cambio en el metabolismo energético que muestran las células tumorales y que hemos mencionado antes y fenómenos de resistencia a la quimioterapia donde parece que el papel de la AMPK puede ser el contrario, favoreciendo esa resistencia al ayudar a las células tumorales a resistir al estrés en el que viven (Wang Z et al. 2016).
Por tanto, mucho queda por investigar y conocer en este importantísimo apartado, pero que parece muy prometedor para el tratamiento de esa enorme lacra que es el cáncer.
Aquí cerramos esta primera parte de la explicación de estas interesantes vías metabólicas. En la segunda parte propondremos cómo equilibrarlas para tener lo mejor de ambas y evitar los efectos negativos de la activación e inhibición de cada una.
BIBLIOGRAFÍA
(1) Thomson DM. The Role of AMPK in the Regulation of Skeletal Muscle Size, Hypertrophy, and Regeneration. Int J Mol Sci. 2018;19(10):3125. Published 2018 Oct 11. doi:10.3390/ijms19103125
(2) Lin SC, Hardie DG. AMPK: Sensing Glucose as well as Cellular Energy Status. Cell Metab. 2018;27(2):299‐313. doi:10.1016/j.cmet.2017.10.009
(3) Ciccarese F, Zulato E, Indraccolo S. LKB1/AMPK Pathway and Drug Response in Cancer: A Therapeutic Perspective. Oxid Med Cell Longev. 2019;2019:8730816. Published 2019 Oct 31. doi:10.1155/2019/8730816
(4) Wang Z, Wang N, Liu P, Xie X. AMPK and Cancer. Exp Suppl. 2016;107:203‐226. doi:10.1007/978-3-319-43589-3_9
(5) Saxton RA, Sabatini DM. mTOR Signaling in Growth, Metabolism, and Disease [published correction appears in Cell. 2017 Apr 6;169(2):361-371]. Cell. 2017;168(6):960‐976. doi:10.1016/j.cell.2017.02.004
(6) Bertoldo MJ, Faure M, Dupont J, Froment P. AMPK: a master energy regulator for gonadal function. Front Neurosci. 2015;9:235. Published 2015 Jul 14. doi:10.3389/fnins.2015.00235
(7) Jeon SM. Regulation and function of AMPK in physiology and diseases. Exp Mol Med. 2016;48(7):e245. Published 2016 Jul 15. doi:10.1038/emm.2016.81
(8) Xu J, Ji J, Yan XH. Cross-talk between AMPK and mTOR in regulating energy balance. Crit Rev Food Sci Nutr. 2012;52(5):373‐381. doi:10.1080/10408398.2010.500245
(9) Johnson SC, Rabinovitch PS, Kaeberlein M. mTOR is a key modulator of ageing and age-related disease. Nature. 2013;493(7432):338‐345. doi:10.1038/nature11861
(10) Kim J, Yang G, Kim Y, Kim J, Ha J. AMPK activators: mechanisms of action and physiological activities. Exp Mol Med. 2016;48(4):e224. Published 2016 Apr 1. doi:10.1038/emm.2016.16
(11) Basualto-Alarcón C, Jorquera G, Altamirano F, Jaimovich E, Estrada M. Testosterone signals through mTOR and androgen receptor to induce muscle hypertrophy. Med Sci Sports Exerc. 2013;45(9):1712‐1720. doi:10.1249/MSS.0b013e31828cf5f3



