Varias ramas dentro de la ciencia de la salud han identificado una serie de procesos conservados, durante los cuales una dosis baja o subletal de un agente o estímulo estresante es capaz de activar una respuesta adaptativa que incrementa la resistencia de una célula u organismo frente a un estrés mucho más severo y muchas veces letal.
Existe una gran cantidad de agentes horméticos entre los que se encuentran la radiación, el calor, los metales pesados, los antibióticos, el etanol, los agentes prooxidantes, el ejercicio y la restricción alimentaria.
Dr. César Montiel – Equipo Médico Neolife
Hormesis y muerte celular
Recientemente, científicos reconocidos en diversos campos publicaron una serie de lineamientos y recomendaciones para unificar el concepto y la terminología para el tipo de respuestas que ocurren en células y organismos al tratar de mantener la homeostasis y adaptarse a un agente tóxico o dañino, y a esta respuesta le llamaron «hormesis» (1).
La hormesis podría definirse como la respuesta ante estímulos que nuestro organismo realiza para sobrevivir ante situaciones adversas. Si la dosis es adecuada obtendremos beneficios, pero si esta no existe o es excesiva tendremos efectos perjudiciales y para determinar este efecto beneficioso o perjudicial debemos entender que los procesos de muerte celular son necesarios para el mantenimiento de la homeostasis que favorece la renovación de tejidos.
Cuando estos mecanismos no se realizan de la manera adecuada se pueden generar enfermedades neurodegenerativas, autoinmunes o incluso células inmortales denominadas cancerígenas, por lo que entendemos que se trata de un proceso beneficioso para la salud. Se ha podido comprobar con experimentos realizados en ratones que eliminando el ATG7 (gen esencial para el desarrollo de la autofagia) los animales morían al poco tiempo de nacer (estudio). El conocimiento actual sobre la muerte celular es bastante limitado, pero recientemente están surgiendo interesantísimas investigaciones que puede aportar en el futuro mucha información sobre su relación con la salud y longevidad.
Los agentes horméticos más importantes que se han identificado a la fecha son la radiación, el calor, los metales pesados, los antibióticos, el etanol, los agentes prooxidantes, el ejercicio y la restricción alimentaria (2,3). La respuesta hormética involucra la expresión de una gran cantidad de genes que codifican para proteínas citoprotectoras como las chaperonas del tipo de las que responden a estrés térmico (heat shock proteins [HSP]), las enzimas antioxidantes, los factores de crecimiento, las metalotioneínas, etc. (4,5). No obstante, todavía no se conocen con exactitud todos los mecanismos y vías de transducción de señales por los cuales la respuesta hormética se lleva a cabo; así, la evidencia experimental sugiere que no existe un mecanismo único sino varias vías que son capaces de desencadenar la hormesis (5,6).
La hormesis originalmente se describió como un fenómeno de dosis-respuesta caracterizado por una estimulación a dosis baja y una inhibición a dosis alta. Es decir, es una relación dosis-tiempo-respuesta en la cual hay una dosis inicial dependiente de una respuesta tóxica, seguida por una respuesta compensadora/rebote (7). Así mismo, la dosis hormética a la cual responde una célula u organismo podrá variar dependiendo del individuo y sus características.
Tipos de muerte celular
La muerte celular está programada y puede durar desde unos pocos días hasta varios años. Cada día, miles de millones de células mueren y los fagocitos las eliminan rápidamente cuando no hay patologías que lo impidan. Sin embargo, este sistema puede verse comprometido cuando gran cantidad de células mueren a la vez (infección, traumatismo o daño tisular) o incluso cuando están sometidas a situaciones insostenibles en el tiempo (inflamación crónica).
Vamos a ver las tres formas más conocidas de muerte celular (estudio).
La muerte es controlada mediante un suicidio celular único propiciado por una acción dirigida por el factor de transcripción p53, la llamaremos apoptosis, al producirse emite señales de “cómeme” para los fagocitos y parece tener un efecto positivo en células vecinas, promoviendo el aclaramiento, acciones antinflamatorias y proliferación celular.
La necroptosis es una forma más agresiva de muerte celular que ha evolucionado de la apoptosis para detectar patógenos y promover la reparación de tejidos. Se produce con un estimulo externo que supone una fuerte agresión y acaba con la célula. Pero en este caso las consecuencias son altamente inflamatorias y efectos negativos para la salud. Esta forma de muerte celular sirve para asegurar la eliminación de células infectadas por patógenos, toxicidad, en casos de enfermedades neurodegenerativas o para inducir el reclutamiento de células fagocíticas al sitio del daño.
Y por último, comentaremos a la piroptosis, que la muerte celular se produce mediante sensores de inflamasoma, que constituyen una fuerte defensa contra patógenos o estrés celular, evitando por ejemplo propagación microbiana. Sin embargo, se puede desencadenar una activación desequilibrada, especialmente relacionada con el NLRP 3 relacionado con una inflamación descontrolada y propiciada, por ejemplo, por la dieta occidental basada en un exceso de comida procesada.
No puedo pasar por alto otro concepto diferente a la muerte celular, como es la autofagia, pero complementario para conservar la salud y longevidad. Se trata de un proceso de reciclaje de componentes celulares con el fin de conseguir la supervivencia de la célula (estudio). En el año 2016 se otorga el Premio Nobel de medicina al biólogo japonés Yoshinori Ohsumi por descubrir los procesos celulares para mantener los niveles de energía y nutrientes en condiciones de inanición o estrés celular.
Este mecanismo sirve a su vez como sistema de control de calidad de orgánulos defectuosos que van surgiendo de manera natural con el envejecimiento. Dentro de las células existen unos orgánulos denominados lisosomas que se encargan de utilizar componentes extras de la célula, que no son vitales para su funcionamiento. De este modo, pueden considerarse plantas de reciclaje para generar sustratos energéticos o nuevas proteínas. Cuanto más activa sea esta función, mayor será la protección de las consecuencias negativas del envejecimiento.
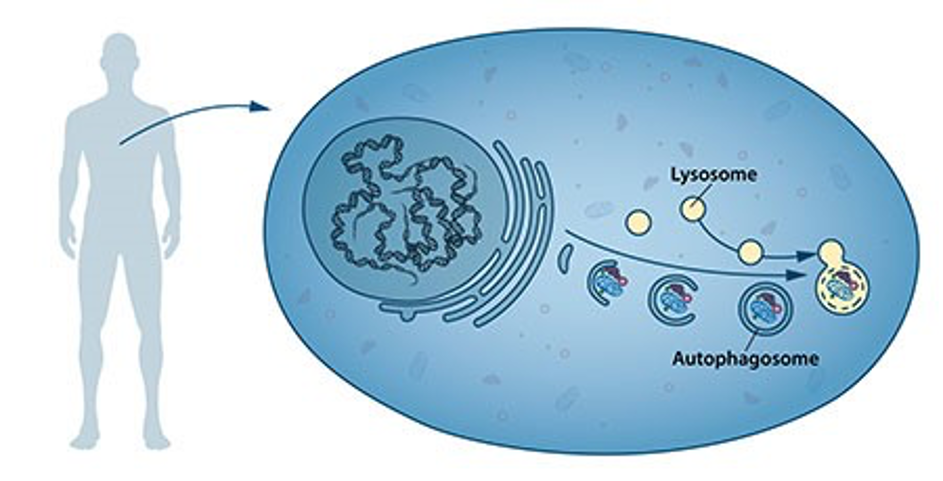
Mitocondrias y dinámica mitocondrial
Las mitocondrias tienen la función de generar energía dentro de la célula y para conseguirlo necesitan optimizar su rendimiento sobre todo en zonas de altísima necesidad energética como las neuronas o miofibrillas del músculo cardiaco. Para conseguirlo tienen mecanismos muy dinámicos que deben permitir mantener este ritmo de flujo constante de energía como la biogénesis mitocondrial (producción de nuevas mitocondrias), procesos de fusión en el que las mitocondrias unen sus membranas y de este modo se permite una complementación genética y fisión mitocondrial que se trata de una división mitocondrial para ofrecer una red ramificada que puede generar energía en todas las regiones pobres en oxígeno (estudio), y durante esta fase ocurre otro proceso llamado mitoptosis que no es mas que un proceso de autofagia especifico de las mitocondrias y supone un importante proceso de eliminación selectiva de mitocondrias dentro de una célula.
Las condiciones de estrés celular por falta de nutrientes o de oxígeno, incluso exceso de radicales libres, aumentan los procesos de dinámica mitocondrial y por tanto de autofagia y mitoptosis. De este modo pueden sacrificarse ellas mismas o parte para producir energía y sobrevivir en condiciones adversas (estudio). Un gran ejemplo para los mamíferos en longevidad es la ballena boreal, superando con facilidad los 200 años y con una resistencia extraordinaria a las enfermedades relacionadas con la edad.
Hace unos años se pudo descifrar el genoma completo de este animal por si daba pistas para que el ser humano aumentara su salud y longevidad (estudio). Pero creo que más que en sus genes, el secreto es su modo de vida y podemos tratar de imitarlo dentro de nuestras posibilidades. Tener pequeños episodios intermitentes de estrés para nuestras células supondrá la base para la longevidad y mantener una buena salud para toda la vida, al igual que hace la ballena boreal.

¿Que estímulos intermitentes podrían ayudarnos?
Hay numerosos estudios que muestran conclusiones favorables de estímulos que podrían favorecer a una buena longevidad, hay uno en especial que lo recomiendo fuertemente articulo. Voy a explicar de forma resumida los principales estímulos sin profundizar mucho en ellos, comenzaremos con el ayuno intermitente, que como ya sabemos, aporta muchos beneficios para la salud si lo hacemos de la forma correcta. La baja variedad de nutrientes de las dietas actuales puede suponer un problema y se asocia con varias patologías (alergias, intolerancias alimenticias, asma, etc.). Las plantas contienen sustancias toxicas naturales para aumentar sus posibilidades de supervivencia que provocan un gran efecto hormético en bajas dosis y beneficiosos en la salud (curcumina, resveratrol, espermidina, etc.). Se ha podido demostrar que una variedad alta de alimentos puede reducir la mortalidad por enfermedad coronaria un 39% y por todas las causas de un 26% (estudio).
Sin embargo, una misma dosis fitoquímica muy continua o incluso en forma de suplemento (excesiva) puede suponer el efecto contrario, bien por exceso de dosis o bien por reducción de beneficios horméticos de otro tipo de sustancias o estímulos importantes. En un ejemplo, se comparó el impacto de un mismo programa de entrenamiento en personas sedentarias con o sin suplementación de 1gr de vitamina C diaria durante 8 semanas. El resultado fue que el grupo sin suplementación tuvo el doble de incremento de VO2max debido posiblemente a la reducción de producción temporal de radicales libres y falta de este tipo de estímulo (estudio).
Tanto el frio y el calor intermitente serian otras dos herramientas de estos estímulos, por ejemplo, el frio es un recurso muy sencillo de utilizar, pero cada vez lo soportamos menos y utilizamos todos los medios posibles para no sentirlo.
El oxígeno es esencial para los humanos y tener niveles mas bajos implica graves consecuencias en la salud, niveles bajos traducen desaturación que en un contexto patológico puede llegar a suponer el aporte externo de oxígeno debido a las consecuencias negativas para el organismo de mantener durante tiempo estos niveles. Sin embargo, la aplicación intermitente de dosis de hipoxia (Hipoxia Intermitente) a la desaturación adecuada ha mostrado grandes beneficios en diversas patologías (metabólicas, cardiovasculares, respiratorias, neurológicas, etc.) por el potentísimo efecto de hormesis en todas las células del cuerpo (estudio). Es posiblemente el estímulo que mas afecta a las células.
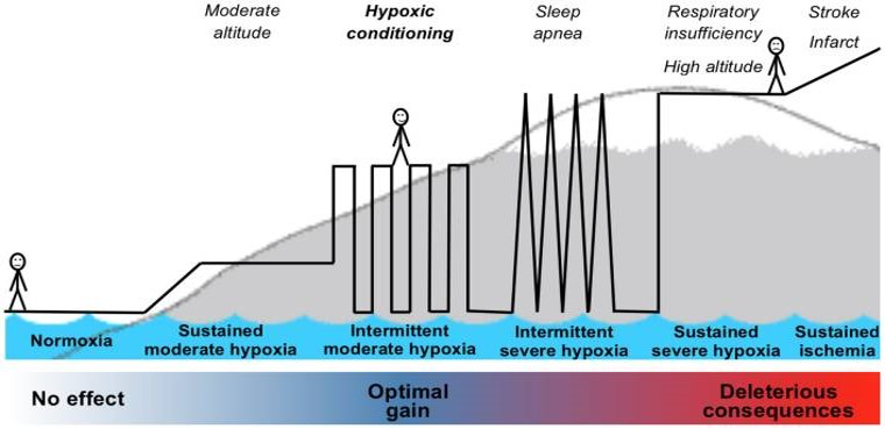
Hormesis y estrés oxidante
De manera escueta y simple, el estrés oxidante puede definirse como un desbalance entre las moléculas oxidantes, principalmente las especies reactivas de oxígeno y de nitrógeno (ERO y ERN) y las moléculas antioxidantes, que favorece a las primeras, generando así un ambiente celular en el cual se propiciará el daño oxidante a las biomoléculas (lípidos, proteínas y ADN) (8,9). Cabe mencionar que el estado redox celular (balance entre el estado oxidado y reducido) es un evento dinámico, que puede cambiar dependiendo de las necesidades fisiológicas de la célula, sin llegar a alcanzar un estado de estrés oxidante.
La constante exposición de los organismos a los cambios ambientales, a la contaminación, a las drogas y los xenobióticos puede generar un incremento en las ERO/ERN, lo que representa una posibilidad de modificar el balance en el estado redox celular, conduciendo al estado de estrés oxidante. No obstante, no solo las interacciones ambientales pueden generar ERO/ERN, también el metabolismo celular normal como la respiración, el estilo de vida, la dieta y la edad son factores que pueden inducir dicho estado. El sistema antioxidante cuenta con compuestos enzimáticos (p. ej. la catalasa, las superóxido dismutasas y las peroxidasas) y no enzimáticos (p. ej. las vitaminas E, C y A y el glutatión reducido), que eliminarán o neutralizarán el exceso de ERO/ERN, evitando así el daño que puedan ocasionar (10). Sin embargo, la respuesta celular de los organismos dependerá de la intensidad del desbalance redox.
Se ha observado que, cuando las células de mamíferos, incluyendo las de humanos, se exponen a dosis bajas de agentes oxidantes, modifican los niveles de expresión de los genes participantes en la respuesta hormética en un intervalo de tiempo aproximadamente de 9 h. Así, la expresión de genes constitutivos, de crecimiento y de proliferación, disminuye, mientras que la expresión de genes protectores aumenta, permitiendo que las células «adaptadas» o «acondicionadas de manera hormética» sean significativamente más resistentes a un estrés oxidante posterior, incluso unas 15 y 30 h después del estímulo inductor (11), así, la respuesta hormética podría semejarse a una respuesta inmune de vacunación; no obstante, a diferencia de esta última, la respuesta hormética no guarda memoria a largo plazo (más allá de las 30 h), y para volver a tener el efecto hormético, las células u organismos deben volver a exponerse al agente inductor.
Se ha propuesto que la respuesta adaptativa antioxidante sea regulada por un complejo sistema de amortiguadores redox, entre los que se encuentran moléculas pequeñas como el glutatión reducido (GSH) y los residuos del aminoácido cisteína presentes en una gran diversidad de proteínas. La cantidad de ellos que se encuentren oxidados le proporcionará información a la célula sobre el estado redox en el que se encuentra. Por ello, la célula emplea el cociente GSH y oxidado (GSSG) y el cociente de cisteína/cistina para evaluar si ha entrado en el estado de estrés oxidante y activar las defensas antioxidantes, todos ellos valorados en nuestra clínica Neolife con el estudio Iimel.
La participación de dichos sistemas amortiguadores redox no solo depende de la magnitud del cambio en el estado redox, sino también de la fase del ciclo o momento metabólico en el que se encuentra la célula. Esta respuesta a la modificación del estado redox de las células se ha observado en diferentes procesos como lo son el envejecimiento, durante el ciclo celular, o en respuesta a ambientes oxidantes (12).
Efecto hormético durante la senescencia y el envejecimiento y la longevidad
El envejecimiento es un fenómeno biológico complejo e inevitable, que se relaciona con el decaimiento o la pérdida de las capacidades fisiológicas, bioquímicas y estructurales de un organismo28, la aparición de las enfermedades relacionadas con la edad son moduladas por la respuesta al estrés oxidante, ya que existe un aumento en la generación de ERO/ERN, principalmente por alteraciones en las funciones bioenergéticas, y una disminución en las vías de reparación y los sistemas antioxidantes 29,30. Los daños generados por este desbalance durante el envejecimiento pueden conducir a desórdenes neurodegenerativos, neoplasias, enfermedades autoinmunes y enfermedades con alteración mitocondrial como la diabetes y el Alzheimer, entre otras.
Muerte celular y estímulos intermitentes
Como hemos visto, la muerte celular es un proceso natural y necesario para mantener la salud, pero se puede realizar de formas diferentes. Unas beneficiosas para la longevidad y salud como la autofagia, mitoptosis y apoptosis, generadas gracias a una dosis hormética intermitente adecuada.
Y otras que son negativas debido a estímulos excesivos como necroptosis (estimulo demasiado agresivo por un patógeno, tóxico o falta de nutrientes). O piroptosis, en la que principalmente por falta de estímulos (muy común en nuestra sociedad), se generar un medio insostenible para las células a largo plazo, que supondrá un estímulo imposible de soportar (alta producción de ROS, inflamación de bajo grado, etc…).
Vamos a resumir de manera muy coloquial para entender todo mucho mejor.
La Mitoptosis es una forma de asegurar la supervivencia de la célula eliminando las mitocondrias defectuosas que muestran su debilidad en momentos de estrés celular. Vamos a entenderlo como una competición de relevos en la que tenemos a un participante de muy bajo nivel que decide retirarse y entregar sus recursos (geles/barritas) a los compañeros.
La Apotosis supone una muerte en paz y calmada de la célula que puede aportar beneficios a células vecinas por utilizar sus recursos. Podría entenderse como la muerte natural de una persona que dona todos sus órganos para que otros puedan sobrevivir en mejores condiciones.
La Necroptosis podríamos entenderla como un asesinato certero de un grupo de células que supone alta producción de ROS y efectos negativos. El ejemplo puede ser un atentado que supone muertes y destrucción cercana generando un problema para todas las células próximas por tener que utilizar recursos para reconstruir el daño.
La Piroptosis implica encontrarse en un medio agresivo para las células, sería como una muerte anunciada en la que la célula se somete a muchas amenazas de las que no puede huir. Esta muerte puede ser en masa y además el mayor problema es que es a nivel sistémico (no localizado) y seguirán existiendo las amenazas en el resto de las células. Sería algo así como un suicidio colectivo de una secta, pero que además puede extenderse porque todos piensan que esa es la única solución al encontrarse en la misma situación.
Resumen
- El estilo de vida moderna nos ha privado de muchos estímulos necesarios para nuestros genes que favorecen la salud y la longevidad, por lo que debemos realizar un esfuerzo por incorporarlos de nuevo en nuestros hábitos.
- La frase “Lo que no te mata te hace más fuerte” ahora tiene una explicación científica. Generar estímulos potentes para nuestras células supone el proceso necesario para conseguir la dosis adecuada de hormesis y, por tanto, la salud con mitocondrias más funcionales y saludables, preparadas para afrontar cualquier desafío con mayor probabilidad de éxito.
- Es fundamental el concepto de estímulo intermitente para que realmente sea terapéutico, debemos dar la dosis necesaria de estímulo y dejar que el cuerpo se adapte para que pueda soportar una dosis aún mayor o por lo menos no perder adaptaciones.
- Nuestros genes tuvieron que soportar durante siglos situaciones de hambre, sed, frio, calor o infecciones. El verdadero problema es dejar de recibir esos estímulos.
- El concepto de alimentación intermitente me parece muy interesante y poco conocido. Se estima que el homo sapiens ha utilizado una dieta de unas 3.000 especies vegetales distintas y la dieta promedio de los humanos modernos es de tan solo 20 (estudio). Tomar un kiwi todas las mañanas puede ser bueno para la salud durante un tiempo, pero tomar solo esa fruta durante 365 días del año me temo que no va a resultar muy saludable. Consumir gran variedad de alimentos (sobre todo vegetales) y de temporada.
- La hipoxia intermitente a pesar de ser el estímulo mas potente, quizá pueda parecer lo mas complejo de aplicar, pero tenemos dos buenas opciones para realizarlo:
- Entrenamiento HIIT, mediante este tipo de estimulo conseguimos una desoxigenación parcial durante un tiempo limitado que ha mostrado grandes beneficios.
- Entrenamientos en hipoxia intermitente con máquina, se puede realizar incluso en condiciones de reposo, siendo el método más cómodo para ofrecer un estímulo muy potente de horméis. Solo necesitas una máquina de hipoxia (cada vez más económica) y un poco de conocimiento.
BIBLIOGRAFÍA
(1) Calabrese EJ, Bachmann KA, Bailer AJ, et al. Biological stress response terminology. Toxicol Appl Pharm. 2007; 222:122-8.
(2) Calabrese EJ, Baldwin LA. Toxicology rethinks its central belief. Nature. 2003; 421:691-2. 7.
(3) Rattan SI. Increased molecular damage and heterogeneity as the basis of aging. Biol Chem. 2008;389:267-72.
(4) Mathers J, Fraser JA, McMahon M, Saunders RD, Hayes JD, McLellan LI. Antioxidant and cytoprotective responses to redox stress. Biochem Soc Symp. 2004;71:157-76
(5) Calabrese V, Cornelius C, Cuzzocrea S, Iavicoli I, Rizzarelli E, Calabrese EJ. Hormesis, cellular stress response and vitagenes as critical determinants in aging and longevity. Mol Aspects Med. 2011; 32:279-304
(6) Zhang Q, Pi J, Woods CG, Jarabek AM, Clewell HJ, Andersen ME. Hormesis and adaptive cellular control systems. Dose Response. 2008; 6:196-208.
(7) Calabrese V, Cornelius C, Dinkova-Kostova AT, et al. Cellular stress responses, hormetic phytochemicals and vitagenes in aging and longevity. Biochim Biophys Acta. 2011;1822:753-83
(8) Sies H. Oxidative stress from basic research to clinical application. Am J Med. 1991;91(Suppl):31-8.
(9) Boveris A, Repetto MG, Boveris AD, Valdez LB. Determinación del estrés oxidativo en seres humanos en situaciones clínicas. En: Königsberg M, ed. Radicales libres y estrés oxidativo. Aplicaciones médicas. El manual moderno. 1.a ed. México: 2008. p. 319-28.
(10) Kowaltowski AJ, Souza-Pinto NC, Castilho RF, Vercesi AE. Mitochondria and reactive oxygen species. Free Radic Biol Med. 2009;47:333-43.
(11) Pickering AM, Vojtovich L, Tower J, Davies KJ. Oxidative stress adaptation with acute, chronic, and repeated stress. Free Radic Biol Med. 2013;55:109-18.
(12) Banerjee R. Redox outside the box: linking extracellular redox remodeling with intracellular redox metabolism. J Biol Chem. 2012;287:4397-402.


